El germen de esta miniserie viene de la primavera de 2020, durante la cuarentena de la primera ola del Covid, período en el que empecé a recibir muchos mensajes al respecto en esa burbuja autoreferencial que es el LinkedIn, en la cual llevo un tiempo muy metido por la situación laboral en una empresa que cerrará sus puertas entre 2021 y 2022, y no por culpa del Covid: la decisión es anterior.
Dada la variedad de artículos que se anunciaban a bombo y platillo en esa red social, empecé a investigar a qué se debía tanto anuncio comercial, y de dónde venía tanta histeria historia. Desde luego la coreografía incluía un elevado cartel de opciones, actores y una gran puesta en escena.
La mayoría de los artículos rezaban sobre el futuro del transporte y cómo éste pasa por el Hidrógeno. Pero no sólo eso. También hablaban mayormente sobre el hidrógeno como elemento de regulación de la producción renovable, mayormente obtenido a partir de agua de mar, y de cómo se estaba trabajando en un rango de vehículos con este combustible.
Así aparecían también un gran rango de anuncios de vehículos de todo tipo: trenes, camiones de gran tonelaje (Iveco, Mercedes, Hyundai, Nikola) y alcance, barcos, aviones (Airbus con tres variantes, nada menos), coches. Que sí el hidrógeno es ‘verde’, que si plantas que aprovechan la energía eólica marina para sacar hidrógeno del mar, que si el transporte del futuro, especialmente camiones, que si meter el hidrógeno en la red de gas natural y así almacenarlo, que si combatir la intermitencia (y la inestabilidad) de las renovables, etc.
Muchos artículos al respecto. Todos ‘chupiguays chachipirulis’, ‘que buenos somos, que tipo tengo’, que ‘me duele la cara de ser tan guapo’… Algunos ya habrán pensado que esto es ‘greenwashing’. Pero es peor.
Así que, aunque ya he escrito sobre este tema, me permito analizar de nuevo y para los casos específicos que se anuncian, todo este entramado de la nueva ‘fiebre del Hidrógeno’, la apuesta europea enorme al respecto, y algunas de las cosas que hay detrás, aunque escribir esta miniserie va a llevar retraso dada la situación personal en que me encuentro.
Hidrólisis.
El hidrógeno, a pesar de ser el elemento químico más abundante de la galaxia, no es algo que tengamos a mano directamente. Siempre, en todos los casos, está combinado con otros elementos químicos, siendo el más habitual, el oxígeno con el que forma agua. Por esa razón, el hidrógeno se debe considerar como un vector de transporte y almacenamiento de energía, no como una fuente de esta, ya que primero se debe obtener, y luego procesar para almacenar y/o transportar. No se ‘recolecta’ como el gas natural o el petróleo, o, ya puestos, una manzana.
Así pues, para poder usar el hidrógeno, primero debemos separarlo del oxígeno con el que conjuntamente forma agua con la archiconocida nomenclatura H2O. El proceso de obtención a partir de agua se conoce como hidrólisis (de hidro, agua, y lisis, separar, dividir), y es relativamente sencilla: se aplica corriente eléctrica ‘continua’, y en un polo se obtiene oxígeno, y en el otro hidrógeno.
Sin embargo, otro elemento común es el metano (gas natural), etano, butano, etc. donde se combina con Carbono (CH4, C2H6, C3H8…). También se obtiene de forma similar, aplicando electricidad, pero lo que se obtiene es hidrógeno y CO2. Actualmente, la mayoría de hidrógeno que se obtiene comercialmente, un 98%, proviene del gas natural, nominal y mayormente, metano. Eso implica que para obtener 1Kg de H2, se obtienen 11Kg de CO2. Y eso sólo por la reacción química, sin contar las emisiones asociadas a otros procesos anexos como la generación de electricidad.
Habida cuenta que un Kg de H2, sobre el papel, ‘tiene’ una energía de 39,9KWh, y que para conseguirlo se ‘gastan’ 4 Kg de metano, que tienen una energía de unos 60KWh (lo que equivale a unas pérdidas de más del 33%), uno se pregunta por qué ese 98% de H2 que se obtiene hoy en día (2020) proviene de gas natural y no de agua. Y encima, perdiendo energía por el camino (ojo, no sólo la química de 20,1 KWh, también la eléctrica que se le ha metido!) a la vez que se emite el CO2.
De hecho, el 3% del consumo de gas natural se usa para obtener hidrógeno, que, en su inmensa mayoría, no se usa precisamente ni para quemar, ni para almacenar (se transforma tal y como se produce, y en el mismo sitio), sino como materia prima para producir amoníaco como precursor de los nitratos, fertilizantes para la agricultura. Eso se lleva el 8,27% de la energía consumida anualmente.
La primera razón que viene a la mente del porqué es obvia, el precio. Y, además, es totalmente acertada. El hidrógeno obtenido de gas natural es más barato que si se obtiene de agua, ya que la diferencia de coste de la electricidad (gasta mucha más la hidrólisis que el proceso Haber-Bosch) es enorme. El precio de un Kg de Hidrógeno listo para usar en el transporte era de unos 14$/Kg (de 12.85 a 16$/Kg), con los cuales el Honda Clarity FCX (Fuel Cell eXperimental) cubre unos 100Km.
Obtenidos a partir de gas natural.
Con eso podemos hacernos una idea del precio que tendrá el hidrógeno obtenido a partir de electricidad, si factorizamos el coste de esta. Este punto, se retomará al final del artículo, porque obviamente, es donde está el tema.
Pero antes, retomemos el tema de la hidrólisis, el proceso para obtener el hidrógeno a partir de agua, porque precisamente es de esto de lo que van los artículos que últimamente están saliendo en los medios de comunicación, bajo la etiqueta de ‘Hidrógeno Verde’, y que vienen a cuento de ciertos planes europeos con inversiones multimillonarias.
La mayoría de estos planes que se anuncian, y que obviamente muchas grandes empresas están interesadas en promocionar (no hay PYMEs en este campo, precisamente, al menos que puedan competir), subrayan que la idea es usar agua de mar para hacer la hidrólisis.
Empecemos por recordar que el agua de mar es sumamente corrosiva. Si metemos electricidad, la cosa empeora. Sin embargo, hay un factor más complejo detrás de todo esto.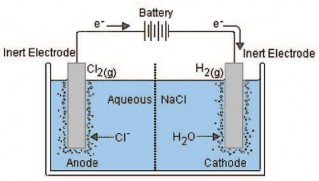
Hace siglos, el que es reconocido como el padre de la química, el francés Lavoisier, desarrolló un método para obtener sosa cáustica disuelta en agua, para así poder hacer jabón (se mezcla con aceite, y se produce la reacción química conocida como saponificación). Obtener sosa cáustica es muy fácil de hacer: se coge agua de mar y se le aplica corriente continua.
¿Les suena de algo?
El resultado que obtenía Monsieur Lavoisier es un concentrado de agua y sosa cáustica, muy alcalino, más una cierta cantidad de hidrógeno (el elemento que se busca en este caso), oxígeno y cloro gaseosos. Eso no sólo eleva la corrosión generada. El impacto ambiental es terrible: se alcaliniza fuertemente el agua de mar de los alrededores, haciendo la zona inhabitable, e incluso se podría llegar a prohibir el baño. A la par, se emite mucho cloro gaseoso a la atmósfera.
Da igual que no se concentre tanto la sosa como con el proceso de Lavoisier. La producción de sosa y cloro es directamente proporcional a la cantidad de hidrógeno generado. Y se está hablando de mucha. (Obviamente, de esto no se dice ni una sola palabra, menos aún ninguna explicación, en los artículos o reportajes que, sin embargo, no se cansan de etiquetar este proceso de ‘verde’, ‘ecológico’, ‘renovable’, etc. Habría que ver esta información cómo será tratada por la nueva ley de censura ‘veracidad’ aprobada. Me la juego a que seguirá igual o incluso más promocionada). Además, el efecto corrosivo que se ha mencionado implica unos elevados costes de mantenimiento. A eso, hay que añadir el coste por ineficiencia. La hidrólisis tiene rendimientos que van del 50 al 70%, y es un tema que ya está bastante estudiado, así que no cabe esperar grandes avances en este sentido.
Es más, esos rendimientos sólo tienen en cuenta la electricidad que se le mete al proceso de hidrólisis, sin contar otros insumos energéticos como el calentamiento del agua (los rendimientos suben con la temperatura), presurización (ídem con la presión), bombeos varios, eliminación de la sosa diluida del proceso, etc. Tampoco tienen en cuenta que el hidrógeno obtenido es de mala calidad, cosa que es sumamente importante para las celdas de combustible (como se verá en el correspondiente apartado), y que hay que purificarlo.
La eliminación del cloro, presumiblemente para volver a meterlo en el agua para reducir el impacto ambiental, es otro insumo que no se tiene en cuenta. Claro que igual lo dejan libre en la atmósfera… Hay que aclarar, para ser honestos, que es precisamente aquí donde hay que trabajar y dónde se pueden dar mejoras (para que el rendimiento, al final, no baje del 50%). Y otro elemento que reduce el rendimiento, es que generalmente estos se suelen dar en condiciones particulares estables de proceso, no en fases de calentamiento, eliminación, procesos por lotes, o variables, intermitentes.
A medida que se reduce la estabilidad del proceso, el rendimiento cae. Todo eso implica, que para obtener un Kg de hidrógeno (recordemos, 39,9 KWh), hay que invertir, en el mejor de los casos, 57 KWh, sin contar otros insumos. Muy probablemente, un valor más realista está entre 60 y 70 KWh, sólo para ese proceso.
Si en lugar de meternos con agua de mar, intentamos hacer la hidrólisis de agua dulce, en un principio nos encontramos con que estamos gastando un recurso que tiene otros usos importantes, como el agua de boca, el regadío, de consumo humano (sanitario) y de ganado, y el mantenimiento de caudales ecológicos de ríos.
Pero es que la hidrólisis de agua dulce generalmente suele pasar por meterle aditivos al agua para mejorar el rendimiento del proceso, obteniendo un residuo que NO es potable y que hay que procesar/eliminar. Así que el impacto ambiental de usar agua dulce es igualmente importante, e igualmente olvidado de forma muy conveniente por los interesados en la materia. No sólo eso. Hasta la fecha, todo proceso de hidrólisis para obtener hidrógeno se ha hecho a partir de agua dulce, porque los catalizadores (aceleradores de la reacción) de agua salada duran poquísimo debido a la cantidad de cosas diferentes que hay en el agua de mar y que los atascan, obstruyen, rompen, saturan, taponan, corroen, etc.
Es decir, se está apostando contra un proceso nuevo que se sabe que es problemático y no rentable (de momento, dirán) en detrimento de un sistema más viejo, conocido y funcional… que tampoco es rentable: recordemos que sigue sin usarse.
A la vista de todo esto, no cabe esperar que el precio del hidrógeno ‘verde’ sea más barato que el del hidrógeno conseguido a partir de gas natural, si bien hay dos elementos que hay que ver cómo se imputan: el coste de la energía metida en el proceso (relacionada con el rendimiento), y las amortizaciones del equipamiento (a saber, no lo pagarán nunca las empresas, puesto que la Unión Europea ya ha decidido que lo pagaremos todos nosotros de nuestro bolsillo, lo usemos o no, haya otras prioridades –como la sanidad, jubilaciones, paro, ayudas al Covid– o no, lo primero son las grandes empresas ‘verdes’ que van a explotar estas inversiones que tan gentilmente les pagamos los currantes de a pie, y que nunca aparecerán en el balance de cuentas, igual que las partidas de mantenimiento).
Por supuesto, habrá que ver exactamente el precio del hidrógeno que se venderá, y a quién se le venderá, y cómo se le venderá. Sobre esto último, más en próximas secciones.
Almacenamiento y transporte.
Como ya traté en su momento, uno de los puntos complicados del manejo del hidrógeno es su almacenamiento y transporte. Hoy por hoy, la gran mayoría del hidrógeno que se produce se gasta en el mismo sitio en que se produce, al mismo ritmo que se produce, y prácticamente en las mismas condiciones (y seguro que en las mismas instalaciones) en que se produce: las plantas de Haber Bosch por las que obtienen amoníaco como precursor de los nitratos de fertilizantes.
Eso implica que no hay ni almacenamiento de hidrógeno puro, y que el transporte, de haberlo, es de unos escasos metros. Y además su uso produce un elemento de elevado valor añadido. Cuando tratamos de usar en diferido el hidrógeno, bien tenemos que almacenarlo, bien que transportarlo a otro lado para su uso. Muy probablemente, ambas cosas a la vez.
Los artículos que se han mencionado hacen referencia a ambas situaciones, si bien, bajo dos contextos diferentes y aplicables a la vez. Por un lado, está el tema de meter el hidrógeno, cuando se produce, dentro de la red de distribución de gas natural (y veremos un ejemplo muy claro e inmediato de interés), donde el almacenamiento es más bien secundario, y además se hace mezclado con el mismo gas natural.
Por otro lado, está el almacenamiento y distribución de hidrógeno para el uso en medios de transporte. Hablan de forma más o menos clara, de su uso en camiones de distribución de grandes tonelajes y distancia, los trailers articulados habituales en nuestras carreteras y que mueven bienes y otras cosas entre países de la Unión Europea o incluso más allá. También entre ciudades relativamente separadas, como pueden ser Madrid, Barcelona, Valencia, Bilbao, Sevilla, La Coruña, Málaga, etc.
Y de trenes, barcos y aviones. Empezaremos por el segundo caso, que es el menos favorable.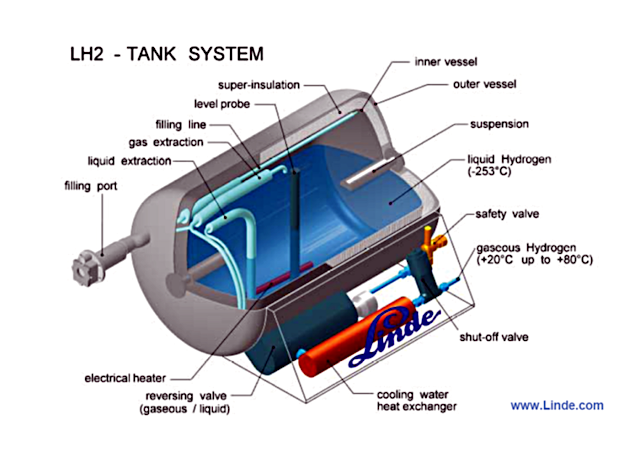
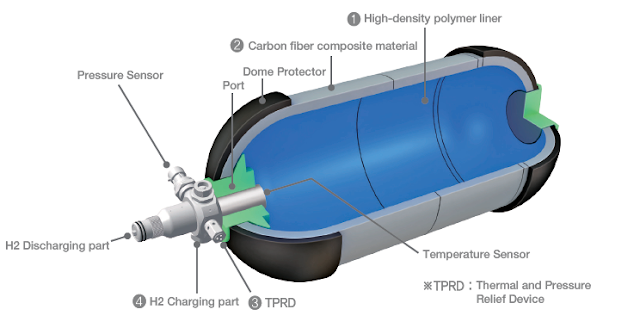
El hidrógeno es una de las moléculas más pequeñas que existen, así que tiene una tendencia muy grande a ‘filtrarse’ a través de paredes y los elementos de contención. Eso obliga a usar capas de forrado interno o ‘liners’ de ciertos materiales que reducen su difusión gaseosa. Pero estos liners no llevan muy bien los cambios de presión y temperatura asociados al proceso de compresión (para el llenado) y descompresión (vaciado) de los depósitos, lo cual obliga a hacer revisiones periódicas.
El transporte del hidrógeno gaseoso a alta presión, como la que se usa para los vehículos eléctricos a celda de combustible, se ha demostrado no ser competitivo debido al peso y volumen del depósito en comparación con la cantidad de hidrógeno, que es muy ligero y poco denso (por eso se usaba para hacer dirigibles, como el Hindemburg).
Por eso, en bastantes casos, el transporte rodado (camión o tren) se hace de forma criogénica, a 20K, es decir -253ºC lo cual hace más factible el transporte a largas distancias, si bien a un coste energético notable para el enfriamiento y licuefacción del hidrógeno, más la posterior regasificación.
Eso para largas distancias. O para almacenamiento local de ‘larga duración’. Algo que reduce aún más la eficiencia. Y causa otra serie de problemas con los materiales utilizados, haciendo los depósitos caros.
Una ‘empresa’ acostumbrada a usar hidrógeno, especialmente en fase criogénica, procura evitarlo en la medida de lo posible, y no se trata de cualquiera, sino de la NASA, que lo utiliza sólo en las etapas de mayores prestaciones de los cohetes. Para el resto, prefieren usar otras cosas como hidrocarburos refinados, o incluso un gas tóxico como la hidrazina antes que el hidrógeno.
Y es que el hidrógeno es un elemento peligroso como para almacenarlo de cualquier manera. Por todo esto, su almacenamiento es bastante complicado, y parece ser que para el caso de vehículos, lo es todavía más para cubrir todos sus requerimientos.
Hay bastante científicos que ante semejante problema, consideran más recomendable el ‘invertir’ más energía y pérdidas para hacer metano sintético, que usar el hidrógeno, ya que es más fácil de almacenar y manejar, por lo que el coste energético por un lado, compensa los problemas que da el hidrógeno en este apartado por el otro.
Entrando más en detalles, el almacenamiento que se está trabajando para vehículos se hace en depósitos a unas 700 atm. Sólo comprimirlo (una vez) a estas presiones, ya implica perder alrededor del 7% de energía. Y hacen falta varias recompresiones, hasta que se alcanzan las 880 atm para poder rellenar el depósito.
Peor aún. Hemos hablado de los liners. Un material habitualmente utilizado para estos fines es el polietileno de alta densidad (HPE, por sus siglas en inglés), que es una variante del plástico usado en las bolsas de súper esas que están prohibidas (suele ser polietileno de baja densidad en ese caso). Y cómo sabemos, los plásticos no son muy amigos de las altas temperaturas. Y al comprimir el Hidrógeno a semejantes presiones, se alcanzan temperaturas de más de 150 ºC, lo cual no es aceptable, especialmente para un liner que no lleva bien el calor, o los componentes orgánicos de los composites necesarios para el depósito.
Así que lo que se hace es enfriar el hidrógeno ANTES de comprimirlo, a 40 ºC bajo cero. Así sólo se llegan a temperaturas de 85 ºC al final del proceso de compresión, unos pocos minutos más tarde. Es decir, en pocos minutos, un depósito pasa de estar vacío metiéndole gas a -40 ºC, a estar sometido a presión, 700 atmósferas, y a 85 ºC.
Si eso no es stress mecánico y térmico…
Obviamente, eso implica que hay que revisar el depósito a menudo para detectar posibles fallas, especialmente en el liner que es el que más sufre el cambio térmico, para reducir posibles fugas del peligroso gas que tiende a acumularse en las zonas altas (es decir, en el techo del habitáculo del coche).
Y probablemente se tenga que sustituir cada cierto tiempo (¿cada 2 años como los catalizadores?) Recordemos que las concentraciones de hidrógeno en aire que son explosivas van del 4 al 75% (el gas natural sólo explota entre 5 y 15% de concentración en aire). Obviamente, si queremos que ese depósito pese poco y ocupe relativamente poco espacio, estamos hablando de que la parte estructural tiene que ser de fibra de carbono, que no es precisamente barata. En cualquier caso, estamos hablando en todo momento de derivados del petróleo o otros elementos fósiles como el carbón.
Y aún así estamos hablando de depósitos que ocupan más de 180 litros, pesan decenas de kilos, 91 kg en el caso del Honda FCX Clarity, para sólo 4 kg de H2, que da como 400 km de autonomía. Y no se puede meter donde uno quiera, ya que tienen que tener forma esférica o cilíndrica para poder soportar tamaña presión. En comparación, un depósito de gasoil de 60 litros ocupa unos 62 litros, con cualquier forma, y pesa menos de 10 kg.
Además, para todo el proceso de almacenaje y distribución, hace falta el ir recomprimiendo el gas varias veces. Primero, para almacenarlo tras la producción. Segundo, para meterlo dentro del camión/barco de transporte que, para las circunstancias, podría llegar a ser incluso un transporte criogénico. Tercero, para meterlo en la estación de recarga (igual hay pasos intermedios, como de barco a camión, antes de llegar a la estación hidrogenera), y, por último, en el vehículo que lo va a gastar.
Dadas las sucesivas recompresiones, con sus respectivas refrigeraciones para evitar temperaturas que dañen el liner prematuramente, estimar las pérdidas sólo en este apartado de presiones en un 10% es ser optimista. Sin hablar de refrigeraciones para transportes criogénicos, las pérdidas relativamente elevadas a esas presiones (del orden del 1% al día).
Tampoco hemos abordado las pérdidas por el propio transporte, por el consumo del vehículo (o los vehículos) que distribuye el hidrógeno generado. Habida cuenta del tamaño y peso del depósito, y que el uso del hidrógeno no es precisamente muy eficiente, el gasto sólo por transporte es bastante más elevado, más del doble, con respecto, por ejemplo, del gasoil.
Por cierto, los barcos a gasoil (mejor dicho, búnker, para hablar con propiedad) tienen un rendimiento del orden del 50%, ya de por sí superior por defecto al del hidrógeno.
Y eso que aún no hemo hablado de cómo se usa…
Celdas de combustible.
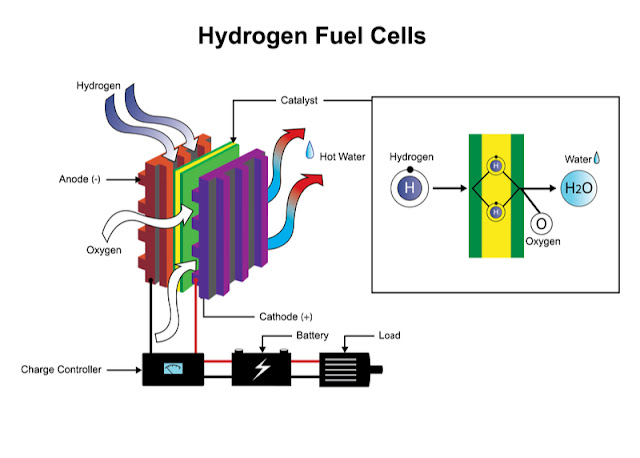 Cuando se habla de usar hidrógeno en el transporte, hay dos modalidades posibles: una es la de ‘quemarlo’ como gas en un motor de explosión, y la otra es la de usar lo que se llama una celda de combustible. ‘Quemar’ hidrógeno en lugar de otro combustible es algo factible con motores que normalmente consumen gasolina (con encendido por chispa, no por compresión como los más eficientes diésel), es decir, vehículos no pesados, y no es algo con un rendimiento espectacular, precisamente.
Cuando se habla de usar hidrógeno en el transporte, hay dos modalidades posibles: una es la de ‘quemarlo’ como gas en un motor de explosión, y la otra es la de usar lo que se llama una celda de combustible. ‘Quemar’ hidrógeno en lugar de otro combustible es algo factible con motores que normalmente consumen gasolina (con encendido por chispa, no por compresión como los más eficientes diésel), es decir, vehículos no pesados, y no es algo con un rendimiento espectacular, precisamente.
El uso de celdas de combustible implica vehículo eléctrico, puesto que dichas celdas, también conocidas como pilas, básicamente convierten el hidrógeno en electricidad al realizar el paso inverso de la hidrólisis. De facto, es exactamente la misma reacción que se produce en las baterías eléctricas de litio, de plomo, alcalinas, de Níquel – hidruro metálico, etc.
La mayor diferencia entre estas últimas y las celdas es que mientras las primeras tienen todo lo necesario para su funcionamiento dentro, incluyendo el ‘combustible’, en las celdas de combustible sólo se tiene la parte que realiza la reacción química propiamente dicha, y en ciertas condiciones, pero no contienen el ‘combustible’, éste es dosificado proveniente de un depósito, y los restos, expulsados a la atmósfera.
Eso tiene un lado positivo: que el ‘combustible’ se almacena de forma separada, así que es muy fácil de recargar, aumentar la capacidad, etc. sin modificar la celda de combustible. Pero tiene un lado negativo: al expulsar el resultado de la reacción química, a saber, vapor de agua (que ya se explicó que es un gas de efecto invernadero), no puede reprocesar éste en una reacción inversa, recuperando así energía, como sí pueden hacer la baterías eléctricas.
Dicho de otra forma, no puede hacer regeneración de energía durante las frenadas o largas bajadas. Además, por la forma y las limitaciones de uso, que hacen que sólo funcione bien dentro de un estrecho margen de potencia, las celdas de combustibles se usan sólo para recargar la batería principal del vehículo. Es decir, no eliminan la batería eléctrica, sólo reducen su tamaño (y precio), aunque eso tiene otras implicaciones como que acortan la vida útil de la misma.
Se está investigando el usar packs de supercondensadores o bacitores en lugar de baterías, lo cual implica un menor peso, una mayor capacidad de potencia y una vida útil más larga, pero no está claro si el precio se va a compensar (no se destina dinero a la investigación de esa vía, seguramente porque ya hay demasiado comprometido con unas baterías de litio para las que este 2020 pronosticaban que una densidad de 1 kWh/kg, cuando en realidad no llegan a los 0,3 kWh/kg, menos de la tercera parte, a pesar de las grandes sumas invertidas).
Por tanto, las celdas de combustible no reducen de forma muy grande el peso del vehículo, ni su volumen, puesto que los depósitos de almacenamiento de H2 son voluminosos, pesados y caros al no haberse alcanzado los objetivos que se habían propuesto alcanzar para estas fechas.
Eso básicamente implica que su uso será más adecuado donde sí se note la diferencia, a saber, en vehículos que necesiten potencia, par y grandes capacidades energéticas difíciles de proporcionar por baterías de litio: los camiones de gran tonelaje y largas distancias. Quién dice camiones, dice trenes en vías sin electrificar, barcos, aviones.
Hay más elementos a tener en cuenta sobre las celdas de combustible. Para empezar, el rendimiento.Ese rendimiento depende de dos factores: la ‘carga’ o % de potencia nominal suministrado, y el tipo de celda de combustible.
| Tipo de Pila | Electrolito | Catalizador | Temperatura de Operación(ºC) | Potencia | Eficiencia Eléctrica(%) | Usos Principales | Ventajas | Inconvenientes |
| PEMFC | polímero sólido | Platino | 80-95 | (0,1-100)kW |
|
|
|
|
| DMFC | polímero sólido | Platino | 50-120 | 1mW-100kW |
|
|
|
|
| AFC | solución de hidróxido de potasio en agua | metales no preciosos | 105-245 | (10-100)kW |
|
|
|
|
| PAFC | Ácido fosfórico líquido | platino sobre base de carbono | 180-205 | >10MW |
|
|
|
|
| MCFC | carbonatos alcalinos sobre una matriz cerámica | material de los electrodos (no platino) | 650 | 100W |
|
|
|
|
| SOFC | sólido cerámico | material de los electrodos (no platino) | 800-1000 | >100kW |
|
|
|
|
La tabla anterior, extraída de la Wikipedia, da una idea de los tipos que existen hoy en día. Los rendimientos de los que habla son rendimientos eléctricos: electricidad suministrada con respecto de la máxima teórica que se podría obtener. Hay ciertas aplicaciones, empero, en las que se ‘añade’ otra eficiencia: la calorífica para producir agua caliente o vapor a baja presión/temperatura, puesto que ciertos tipos trabajan por encima de los 600ºC.
Entre los diferentes tipos, hay algunos que son muy delicados, y otros que son robustos. Hay muchos que utilizan metales preciosos como catalizador (habitualmente platino), y los hay que no. Y los hay que utilizan tierras raras (habitualmente Lantano, el más común de estos elementos químicos, pero además suelen usar Itrio, otro elemento que no es una tierra rara, pero que se le considera como tal), y los hay que no.
También los hay que trabajan a temperatura ambiente, y los que trabajan ‘en caliente’.
Vamos, que hay variedad.
Resulta que hay uno que es muy estimado por la industria, llamado SOFC, (celda de combustible de óxido sólido, y la MFC que es muy parecida), que tiene un gran rendimiento tanto eléctrico como calorífico… porque trabaja a más de 600ºC, no usa metales preciosos, es muy robusto en frente a la calidad del gas o incluso otros elementos usados para producir electricidad (hay variantes que usan metanol, metano, etc) y es relativamente durable, es decir, no hay que cambiarlo tan a menudo como otros tipos.
Sólo que trabaja a más de 600ºC, tarda una hora en calentarse al punto de trabajo necesario, utiliza tierras raras como el Lantano, Estroncio, Cerio y el mencionado Ytrio, a veces también Zirconio… todos ellos elementos que tampoco son baratos pero sí escasos, si bien tanto el Lantano como el Cerio son subproductos de extraer Neodimio y Disprosio, que son necesarios para el motor que tiene que mover a estos vehículos, o los grandes aerogeneradores de gran potencia.
Aún así, el rendimiento de la celda está en el 60% a régimen estable (justo lo que no tienen los motores de los vehículos, un régimen estable) sin contar las pérdidas por otros elementos, como sería en el caso de un camión, la refrigeración del calor sobrante, por la caída de presión del depósito de combustible, o el consumo de combustible durante una hora para ponerlo a la temperatura de trabajo… Y lo que se pierde por la intermitencia de ir cargando la batería con períodos de no cargarla.
Hay otros que serían más adecuados para usar en coches incluso, sin problemas de calentamiento (trabajan a temperaturas bajas, incluso a temperatura ambiente), son menos voluminosos (no hay que enfriarlos), y no utilizan tierras raras… utilizan platino, y duran poco, haciéndose necesario el cambio del catalizador de platino cada dos años… si la mala calidad del gas suministrado no lo estropea antes.
Y eso sin mencionar que, en muchos casos, la concentración de oxígeno no es suficiente y como mínimo hay que comprimir el aire (para aumentar la cantidad de O2 presente en la celda y obtener el rendimiento establecido), por no decir que hay que llevarlo encima, de forma pura (sin el >70% de N2 que tiene nuestra atmósfera) y comprimida dentro de una bombona.
Algunas sólo quieren trabajar con oxígeno puro o aire muy purificado, como la AFC. Sea el caso que sea de estos dos últimos, es otra bajada (encubierta, no contabilizada) del rendimiento, ya que hay que comprimir, y probablemente separar el oxígeno, más el problema de que consumimos más porque tenemos que llevar más peso, otro depósito, etc. Eso, o el rendimiento de la celda cae mucho debido a la falta de oxígeno. Cosa que se acentúa con las alturas (subidas a montañas, localidades muy por encima del nivel del mar, como México capital), etc. Por no hablar de posibles fallos catastróficos por contaminación por CO2, por ejemplo.
El mejor de los casos, contando solo pérdidas de electrólisis siendo ésta óptima (70%) y una pila de combustible en el punto óptimo (60%), tenemos un rendimiento del 42%. Si sumamos las pérdidas por la gestión y el almacenamiento del hidrógeno, el rendimiento no va a superar nunca un 30% real y efectivo.
Pésimo.
En comparación, un vehículo a batería puro tiene un rendimiento de más del doble, por encima del 70%. Eso implica que hay que producir como mínimo más del doble de la electricidad de origen renovable que usando vehículos a batería pura.
Y todo, para tener algo de almacenamiento, reducir algo el peso de los vehículos, ahorrar algo en unas caras, voluminosas y pesadas baterías, y así tener la posibilidad de vehículos pesados de transporte que de otra forma serían inviables. Amén de facilitar la recarga. Decir que semejante opción es el futuro quiere decir una de dos cosas: o que no saben de qué están hablando, o que ya dan por imposibles los camiones de gran tonelaje a batería, como ya dijo Bill Gates… y algunos más.
Lo más probable: ambas cosas.
Resumiendo:
- Un vehículo a celda de combustible no elimina la batería, sólo la reduce.
- Con ello, acorta la vida útil de dicha batería, aunque se puede utilizar una de LiFePO que dura más, con mayor peso, precio por kWh, volumen, y menor rendimiento al necesitar un 20% más de litio que las utilizadas comúnmente, y que no tienen margen de mejora apenas pues están ya a un 98% del rendimiento teórico máximo.
- El peso y volumen del depósito de hidrógeno apenas compensa la diferencia de peso.
- Las soluciones actuales utilizan materiales escasos y caros, y tienen sus inconvenientes para este tipo de aplicación.
- El bajo rendimiento implica que hace falta mucha más generación eléctrica. Y más capacidad debido a que no puede regenerar energía en tantos casos como las baterías.
- La infraestructura de recarga, aunque en apariencia sencilla de transformar, no lo es tanto, y la logística de reparto es otro problema añadido que implica utilizar muchísima más energía que se pierde en comparación con otras opciones.
- El precio está por ver, pero todo apunta a que no será más competitivo que las caras baterías.
- Con estos datos, no parece para nada viable esta opción, especialmente para vehículos ligeros y coches. Y quién lo dice esta vez, es alguien con interés en el tema de vender vehículos: VW.

Los comentarios están cerrados.